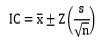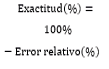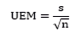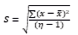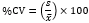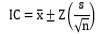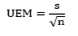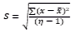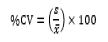Development and Implementation of an Open-Source Potentiometric Device for Teaching Hydrogen Potential (pH)
Abstract
This study developed an open-source potentiometric device for measuring pH, intended as a resource for chemistry education. The device was assembled using an Arduino Nano board, a pH sensor, a temperature module, and other components that provided portability and data transmission capabilities. Calibration was performed using reference solutions of potassium biphthalate (KHC₈H₄O₄) and monobasic and disodium potassium phosphate (KH₂PO₄ and Na₂HPO₄). pH measurements were conducted on everyday-use solutions to evaluate the device’s stability through parameters such as linearity, precision, accuracy, robustness, and uncertainty. For the pedagogical component, a quasi-experimental design with pretest-postest measurements was applied to 29 undergraduate students in Natural Sciences and Environmental Education, divided into an experimental group and a control group. The experimental group participated in theoretical-practical sessions focused on the concept of pH and the device assembly, while the control group received traditional instruction. Statistical analysis using Chi-square and Fisher’s exact tests showed improvements in the experimental group, although no statistically significant differences were found between the two groups.
Keywords: pH; hydrogen; potentiometry; teaching, chemistry; Arduino
Desenvolvimento e implementação de um equipamento potenciométrico de código aberto para o ensino do potencial de hidrogênio (pH)
Resum0
Este estudo desenvolveu um equipamento potenciométrico de código aberto para medir o pH e utilizá-lo como recurso no ensino da Química. O dispositivo foi montado com uma placa Arduino Nano, sensor de pH, módulo de temperatura e outros componentes que proporcionaram portabilidade e transmissão de dados. O equipamento foi calibrado com soluções de referência de biftalato de potássio (KHC₈H₄O₄) e de fosfato monobásico e dibásico de potássio e sódio (KH₂PO₄ e Na₂HPO₄). Foram realizadas medições de pH em soluções de uso cotidiano, a fim de avaliar a estabilidade do equipamento por meio dos parâmetros de linearidade, precisão, exatidão, robustez e incerteza. No componente pedagógico, aplicou-se um delineamento quase-experimental, com mensuração pré-teste e pós-teste, envolvendo 29 estudantes do curso de Licenciatura em Ciências Naturais e Educação Ambiental, distribuídos em grupo experimental e grupo de controle. O grupo experimental participou de sessões teórico-práticas voltadas ao conceito de pH e à montagem do equipamento, enquanto o grupo de controle recebeu instrução tradicional. A análise estatística, por meio dos testes do Qui-quadrado e Exato de Fisher, indicou melhorias no grupo experimental, embora sem diferenças estatisticamente significativas entre os grupos.
Palavras-chave: pH; hidrogênio; potenciometria; ensino; química; Arduino
Introducción
El potencial de Hidrógeno (pH) es una magnitud fisicoquímica de gran relevancia para comprender procesos celulares (Aoi & Marunaka, 2014), diagnosticar y tratar enfermedades (Antończyk et al., 2023), evaluar la biodisponibilidad de nutrientes en el agua (Samešová et al., 2023), regular reacciones químicas (Zhang et al., 2023), controlar la actividad microbiológica y enzimática (Dey & Sheth, 2023), determinar la presencia de metales pesados en los suelos y el agua (Kicińska et al., 2022), eliminar compuestos contaminantes (Li et al., 2023) e identificar las características químicas de materiales que pueden ser empleados en la industria (Simha et al., 2023). En general, todos los procesos químicos, biológicos y bioquímicos dependen del pH, razón por la cual, esta medida es universalmente trascendental en el campo científico y tecnológico (Khan et al., 2017).
El pH puede ser medido por el método de colorimetría, en el cual se emplean indicadores como el papel tornasol o el papel de pH, que cambian de color de acuerdo a la naturaleza química de la solución en que se introduzcan (Khan et al., 2017); a pesar de que este método es económico y práctico, su principal limitante es que es inexacto y solo debe usarse como una medición semicuantitativa (Gill & Zheng, 2020). Otro método es el óptico, en el que se emplean sensores constituidos por polímeros o colorantes que presentan una respuesta óptica de absorción o emisión que depende del pH; aunque garantiza respuestas rápidas, sin contacto y sin utilizar condiciones especiales de almacenamiento, presenta limitaciones debido al fotoblanqueo, extinción de la fluorescencia y lixiviación o fuga de los colorantes (Bartoš et al., 2022; Khan et al., 2017).
Las dificultades presentadas en estos métodos impiden obtener resultados fiables y trazables, afectando la toma de decisiones relacionadas con este parámetro (Hindayani et al., 2021). Por el contrario, el método de potenciometría es considerado como el más idóneo, porque su indicación del valor del pH se deduce de la diferencia de potencial entre un electrodo sensor de pH y un electrodo de referencia (Cristancho & Castillo, 2020). Según la IUPAC, el valor de pH se define en términos de la actividad del ion hidrógeno H+ en una solución acuosa () (Buck et al., 2002). Sin embargo, debido a que la medida es difícil de determinar individualmente, es necesario calibrar los instrumentos potenciométricos con Materiales de Referencia Certificados (MCR) para garantizar datos confiables (Cristancho & Castillo, 2020).
Una de las razones por las cuales las medidas de pH no siempre garantizan su confiabilidad y trazabilidad con el Sistema Internacional de Unidades (SI) es el elevado costo de los materiales de referencia, lo cual limita su accesibilidad (Hindayani et al., 2021). Además, los dispositivos potenciométricos pueden costar entre $800 000 y $7 500 000 COP, lo que resulta inaccesible para agricultores, agrónomos, pequeños empresarios, estudiantes e investigadores que miden este parámetro regularmente (Zambrano et al., 2019). A esto se suma que algunos instrumentos presentan limitaciones para almacenar y transmitir datos o corregir el valor de pH según la temperatura del analito (Julian, Wahyuni & Ulhaq, 2023).
En el ámbito educativo, el concepto de pH ha enfrentado diversas dificultades debido a su uso inadecuado en textos que omiten fundamentos teóricos y operativos, y a una definición desactualizada basada en la concentración de iones de hidrógeno, en lugar de la moderna, que se basa en la actividad de estos iones (Lunelli & Scagnolari, 2009; Mccarty & Maynard, 2006). Además, el enfoque exclusivamente teórico y matemático hace que el concepto resulte poco atractivo para los estudiantes (Pineda et al., 2020).
Los procesos de enseñanza influyen directamente en la correcta medición del pH. Sin embargo, en la práctica, comúnmente se cometen errores como el uso inadecuado del electrodo en seco, limpieza incorrecta del bulbo, empleo de soluciones inapropiadas para la limpieza de los electrodos, incorrecta inmersión de la sonda y uso de electrodos antiguos o expirados (Grupo Hanna Instruments, 2020). Adicionalmente, los estudiantes tienen pocas oportunidades para ensamblar y comprender cómo funcionan los instrumentos de medida (Santos & Cavalheiro, 2015), lo cual trae consigo el desconocimiento en la instrumentalización y automatización del análisis químico moderno.
Por lo anterior, esta investigación abordó dos aspectos problemáticos: las limitaciones de los equipos y procedimientos convencionales para la medición de pH, y los desafíos en su enseñanza, especialmente en lo relacionado con el enfoque conceptual y la limitada articulación entre teoría y práctica. En este contexto, se diseñó un equipo potenciométrico de código abierto, ensamblado con una placa Arduino Nano, un sensor de pH DFRobot Gravity V2 y otros módulos. El sistema fue calibrado utilizando patrones de referencia del Instituto Nacional de Metrología de Colombia (INM) y empleado para realizar mediciones en soluciones de uso cotidiano.
En el componente pedagógico, se aplicó un diseño pretest-postest con 29 estudiantes del programa de Ciencias Naturales y Educación Ambiental, distribuidos en un grupo experimental (n=12) y uno de control (n=17). El grupo experimental participó en talleres teórico-prácticos sobre el concepto de pH y el ensamblaje del equipo potenciométrico, mientras que el grupo de control recibió únicamente clases tradicionales.
Metodología
Esta investigación se enmarcó en el paradigma hipotético-deductivo, ampliamente utilizado en las ciencias naturales para establecer relaciones causa-efecto y generalizar casos específicos (Ricoy, 2006). En el ámbito educativo, este enfoque permite consolidar conocimiento empírico mediante métodos cuantitativos y procedimientos controlados para analizar fenómenos en el aprendizaje de las ciencias (Sánchez, 2019). Además, este estudio adoptó un diseño experimental, porque se manipularon variables y se controló la muestra, tanto en el enfoque disciplinar como en el pedagógico.
Componente disciplinar
Este componente implicó el diseño del equipo potenciométrico, su calibración con MRC proporcionados por el Instituto Nacional de Metrología y medición de pH con soluciones de uso cotidiano. A continuación, se describen las etapas metodológicas de este componente.
- Etapa 1: Preparación del equipo potenciométrico
Se configuraron las conexiones de los sensores de pH y temperatura en el prototipo, y se estableció la comunicación entre el software y el hardware mediante un código de programación en Arduino, garantizando el funcionamiento integrado del sistema.
- Etapa 2: Calibración del equipo potenciométrico
Se programó el Arduino para ejecutar la calibración del sensor de pH, comenzando con una limpieza del sensor y sumergiéndolo en las soluciones de referencia: biftalato de potasio (KHC8H4O4) con un pH de 4,01 a 25° C y fosfato de potasio monobásico y fosfato di sódico (KH2PO4 y Na2HPO4) con un pH de 6,86 a 25° C. A través de comandos en el monitor serial, se configuraron y almacenaron puntos de calibración, permitiendo ajustar el código según las lecturas estables de pH.
- Etapa 3: Pruebas de medición
Los sensores fueron limpiados y sumergidos en soluciones de vinagre (SA), hidróxido de agua (SN) e hidróxido de magnesia (SB) para registrar lecturas de pH con y sin compensación de temperatura. Las pruebas de medición se repitieron durante 30 días en dos laboratorios con condiciones ambientales distintas; los primeros 20 días en uno y los 10 días restantes en otro.
- Etapa 4: Validación del equipo
Se evaluaron parámetros clave del instrumento, incluyendo su linealidad, precisión, exactitud, robustez e incertidumbre, con el propósito de validar el rendimiento y la confiabilidad del equipo diseñado.
Componente pedagógico
Este componente utilizó un diseño experimental de pretest-postest con dos grupos, uno experimental y uno de control; el grupo experimental recibió el tratamiento, mientras que el grupo de control no. Se realizó una medición final para analizar las diferencias entre el pretest y el postest y determinar los efectos del tratamiento. La muestra fue seleccionada de forma no aleatoria y por conveniencia, la cual consistió en 29 estudiantes de Licenciatura en Ciencias Naturales y Educación Ambiental de la Universidad Pedagógica y Tecnológica de Colombia, que cursaban la asignatura de Química Orgánica en el año 2024; de ellos, 17 integraron el grupo de control y 12 el experimental. Las fases de este componente fueron:
Fase 1. Diagnóstico (Pretest)
Se identificaron algunos conocimientos de los estudiantes en relación al concepto de pH, SI y metrología química del pH, para ello, se diseñó y validó un pretest de 10 preguntas, el cual también se implementó como postest en la fase de evaluación, tal como se puede observar en la tabla 1.
Tabla 1. Estructura pretest y postest.
|
Pregunta
|
Opción de respuesta
|
Objetivo de la pregunta
|
|
1. Según la IUPAC, la definición teórica del pH es:
|
a) El logaritmo negativo de la concentración de iones de hidrógeno y que se puede representar con la ecuación log [H+].
b) El logaritmo negativo de la actividad del ion hidrógeno y que se puede representar con la ecuación log aH+.
c) El logaritmo negativo de la concentración de iones hidroxilo y que se pueden representar con la ecuación log [OH˗ ].
d) El logaritmo negativo de la actividad del ion hidroxilo y que se puede representar con la ecuación log a[OH˗].
|
Evaluar la comprensión conceptual del pH desde una perspectiva moderna
|
|
2. De acuerdo con la Guía de Medición del pH. Definiciones, estándares y procedimientos de la IUPAC el Sistema Primario de medición del pH se realiza con una celda de Harned. Esta celda está constituida por un electrodo de platino platinizado (Pt/H2) y un electrodo de plata/cloruro de plata (Ag/AgCl), por lo tanto, su principio de funcionamiento se basa en el método de:
|
a. Colorimetría.
b. Potenciometría.
c. Espectrometría.
d. Óptico
|
Identificar los principios fundamentales del sistema primario de medición del pH.
|
|
3. Para calibrar un electrodo de pH se mide el potencial del electrodo en soluciones buffer de pH conocido y se grafica el potencial medido en función del pH. La pendiente de la línea obtenida en este gráfico corresponde a la pendiente de Nernst, la cual teóricamente debe ser aproximadamente de:
|
a. 59,16 mV/pH a 20°C
b.-59,16 mV/pH a 20°C
c.-59,16 mV/pH a 25°C
d. 59,16 mV/pH a 25°C
|
Relacionar el proceso de calibración de un electrodo de pH y su relación con la ecuación de Nernst
|
|
4. El concepto de trazabilidad metrológica del pH puede asociarse como una:
|
a. Propiedad de un resultado de medida, el cual puede relacionarse con un valor de referencia del pH mediante una cadena ininterrumpida y documentada de calibraciones.
b. Proximidad entre los valores de pH obtenidos en mediciones repetidas de una misma solución bajo condiciones especificadas.
c. Propiedad de un instrumento de medida de pH que conserva constantes sus características metrológicas a lo largo del tiempo.
d. Curva de calibración del pH que muestra la relación entre el valor medido por un electrodo de pH y los valores de pH conocidos de soluciones de referencia.
|
Reconocer el concepto de trazabilidad metrológica en el contexto de la medición del pH.
|
|
5. Suponga que una sonda de pH es calibrada con soluciones de referencia de 4,01 y 7,00. Si en la solución de pH 4,01 el sistema mide un potencial de 173 mV y la de pH 7,00 mide un potencial de -3,1 mV, indique cuál es la ecuación que representa la pendiente de calibración (Ŝ).
|
|
Emplear correctamente la fórmula de cálculo de la pendiente de calibración (Ŝ) de un electrodo de pH.
|
|
6. En un laboratorio de química se realizó una calibración con soluciones de referencia de pH 4,01 y 7,00 a 25° C. Las muestras fueron almacenadas en un lugar fresco, para luego, medir su pH a 10° C. Lo que se espera de este procedimiento es que:
|
a) El valor de pH de las soluciones será el mismo a 10° C y a 25° C, porque el pH es independiente de la temperatura.
b) El valor de pH de las soluciones no será el mismo a 10° C y a 25° C porque el pH es dependiente de la temperatura.
c) La temperatura no afectará la solución de 7,00 pero sí, la solución de pH de 4,01, porque el pH es dependiente de la temperatura cuando la solución es ácida.
d) La temperatura no afectará la solución de 4,01 pero sí, la solución de pH de 7,00, porque el pH es dependiente de la temperatura cuando la solución es neutra.
|
Identificar el pH como una magnitud dependiente de la temperatura.
|
|
7. Un equipo potenciométrico -llamado comúnmente pH-metro- es un dispositivo utilizado para medir el pH de una solución. Este dispositivo incluye varios componentes esenciales para realizar medidas precisas, entre ellos, un electrodo de referencia, el cual tiene por función principal:
|
a) Generar una señal eléctrica proporcional al pH de la solución.
b) Proporcionar un punto de referencia estable para la medición del potencial eléctrico.
c) Detectar la actividad de los iones hidrógeno (H+) en la solución.
d) Mantener estable la temperatura de la solución durante la medición.
|
Reconocer la función principal del electrodo de referencia en un sistema potenciométrico.
|
|
8. Aunque el pH es una medida adimensional, sí presenta una estrecha relación con unidades como el mol. Teniendo en cuenta que con la última redefinición de unidades del SI cada unidad se encuentra asociada a una constante, indique a qué constante se encuentra asociado el mol:
|
a. A la constante de Boltzmann.
b. A la constante de Avogadro.
c. A la constante de Planck.
d. A la carga elemental.
|
Reconocer la constante física fundamental asociada a la unidad de cantidad de sustancia (mol) en el Sistema Internacional de Unidades (SI).
|
|
9. De acuerdo con el “Vocabulario Internacional de Metrología, conceptos fundamentales y generales y términos asociados” la incertidumbre de medida se define como: “un parámetro que caracteriza la dispersión de los valores atribuidos a un mensurando, a partir de la información que se utiliza”. Cuando la incertidumbre es evaluada estadísticamente a partir de las mediciones directas, se llama:
|
a. Incertidumbre de tipo A.
b. Incertidumbre de tipo B.
c. Incertidumbre cuadrada.
d. Incertidumbre triangular.
|
Identificar el tipo de incertidumbre según su método de evaluación, de acuerdo con el Vocabulario Internacional de Metrología (VIM).
|
|
10. Asuma que realizó una práctica de laboratorio donde utilizó un equipo potenciométrico para medir el pH de una Solución de Referencia Certificada de 4,01 y otra de 10, realizando 5 réplicas por cada solución, tal como aparece en la siguiente tabla:
|
Solución de referencia pH 4,01
|
Solución de referencia pH 10
|
|
4,01
|
8,01
|
|
4,01
|
8,02
|
|
4,02
|
8,03
|
|
4,03
|
8,02
|
|
4,01
|
8,01
|
De acuerdo a los resultados es correcto afirmar qué:
|
a. Las medidas realizadas con la solución de 4,01 demostraron precisión y las de la solución de 10 unidades de pH demostraron exactitud.
c. Las medidas realizadas con la solución de 4,01 demostraron exactitud y las de la solución de 10 unidades de pH demostraron precisión.
b. Las medidas realizadas con ambas soluciones demostraron exactitud.
c. Las medidas realizadas con ambas soluciones no demostraron exactitud.
|
Diferenciar los conceptos de precisión y exactitud a partir de un conjunto de datos obtenidos mediante mediciones repetidas del pH.
|
Fuente: elaboración propia
Fase 2. Intervención
En esta fase, el grupo de control recibió dos sesiones teóricas, mientras que el grupo experimental tuvo una sesión teórica y otra práctica. Las sesiones teóricas cubrieron conceptos de pH, jerarquía de medición, relación con el SI, y calibración de sensores. La sesión práctica permitió al grupo experimental contextualizar estos conocimientos mediante el diseño de equipos potenciométricos de código abierto, similares al propuesto en el componente disciplinar de este estudio.
Fase 3. Evaluación (Postest)
Después de la intervención, se aplicó un postest para evaluar los conocimientos adquiridos por los grupos control y experimental. Las frecuencias de respuestas correctas se compararon mediante el modelo Chi² con corrección de Yates y, cuando los valores esperados superaban 5 en el pretest y postest, se usó la Prueba Exacta de Fisher. Estos análisis permitieron determinar, mediante el valor p, si existían diferencias significativas en las respuestas correctas entre ambos grupos.
Resultados y discusión
Diseño del equipo potenciométrico
El equipo potenciométrico diseñado en esta investigación empleó un sensor analógico de pH DFRobot Gravity V2, un sensor de temperatura sumergible DS18B20, una resistencia de 4,7Ω, un módulo de carga Tp4056 USB Tipo C, una batería de litio recargable de 3,7v 1000 mAh, una unidad de microcontrolador Arduino nano V.3, un módulo Bluetooth HC-05, cables jumpers macho-hembra y macho-macho, baquelita e hilo de estaño. Las conexiones fueron soldadas de acuerdo a la siguiente figura:
Figura 1. Conexiones del equipo potenciométrico de código abierto (hardware).
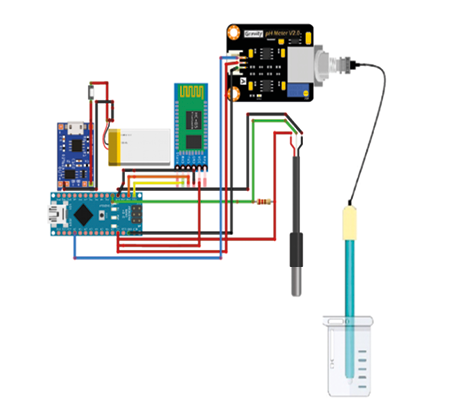
Fuente: Elaboración propia.
Este circuito permitió medir el pH de diversas soluciones con gran flexibilidad, ya que incluyó un módulo de conexión inalámbrica, puerto mini USB, batería de litio y sistema de carga, lo cual favoreció su portabilidad. El microcontrolador Arduino Nano se programó en la versión 2.3.0 de Arduino IDE, ejecutado en un equipo Dell con Windows 10. Los datos fueron visualizados en el monitor serial, utilizando librerías como EEPROM, OneWire, DallasTemperature y DFRobot_pH para interpretar la información de los sensores.
Validación del equipo potenciométrico
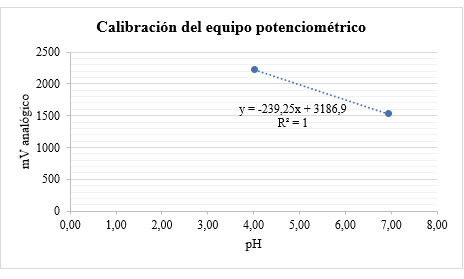
La linealidad del equipo potenciométrico se determinó a través de una regresión lineal, descrita a partir del promedio de pH calibrado durante los 30 días para cada una de las soluciones de referencia y los mV analógicos del equipo, tal como aparece en la tabla 2. Por otra parte, en la figura 2 se evidencia la curva y ecuación de calibración del equipo.
Tabla 2. Promedio de pH y Voltaje para MCR
|
MCR
|
pH calibrado
|
Voltaje
|
|
MCRn
|
4,02
|
2225,09
|
|
MCRa
|
6,93
|
1528,87
|
Fuente: elaboración propia
Figura 2. Relación pH/ mV analógicos
Fuente: Elaboración propia.
Los resultados muestran que las mediciones fueron lineales, con un R² de 1, lo que indica que los datos se ajustan perfectamente a una línea recta. La ecuación de calibración obtenida fue y=−239,25x+3186; la pendiente negativa sugiere que, a menor pH, el voltaje analógico aumenta, mientras que, a mayor pH, disminuye. Cabe señalar que los mV analógicos provienen de la salida del circuito y no directamente del electrodo, donde se esperaría un voltaje de 414,12 mV para un pH de 0 y -414,12 mV para un pH de 14 (Alzate et al., 2012).
A continuación, se presentan los resultados de precisión, robustez, exactitud e incertidumbre de medida para las soluciones de referencia (MCRa y MCRn) y las soluciones de uso cotidiano (SA, SN, SB). La tabla 3 muestra los resultados obtenidos en el laboratorio 1, correspondientes a los primeros 20 días de estudio, mientras que la tabla 4 incluye los resultados del laboratorio 2, obtenidos durante los últimos 10 días de estudio.
Tabla 3. Resultados de medición de pH- Laboratorio 1.
|
Resultados medición de pH Laboratorio 1
|
|
Precisión
|
Robustez por Intervalo de Confianza (99%)
|
% Exactitud
|
Incertidumbre Estándar de Medida (UEM)
|
|
Desviación estándar
|
Coeficiente de variación
|
|
Límite inferior del Intervalo
|
Límite superior del Intervalo
|
|
MCRa
|
0,13
|
3,26
|
2,45
|
2,68
|
99,24
|
0,03
|
|
MCRn
|
0,13
|
1,87
|
6,94
|
7,32
|
98,88
|
0,03
|
|
SA
|
2,45
|
7,7
|
2,68
|
2,45
|
N/A
|
0,04
|
|
SN
|
6,94
|
4,6
|
7,32
|
6,94
|
N/A
|
0,07
|
|
SB
|
9,69
|
2,7
|
10,00
|
9,69
|
N/A
|
0,06
|
Fuente: elaboración propia
Tabla 4. Resultados de medición de pH- Laboratorio 2
|
Resultados medición de pH Laboratorio 2
|
|
Precisión
|
Robustez por Intervalo de Confianza (99%)
|
%Exactitud
|
Incertidumbre estándar de medida (UEM)
|
|
Desviación estándar
|
Coeficiente de variación
|
|
Límite inferior del Intervalo
|
Límite superior del Intervalo
|
|
MCRa
|
0,15
|
3,75
|
2,59
|
2,83
|
97,99
|
0,05
|
|
MCRn
|
0,11
|
1,52
|
7,28
|
7,64
|
99,14
|
0,03
|
|
SA
|
0,15
|
5,53
|
2,59
|
2,83
|
N/A
|
0,05
|
|
SN
|
0,22
|
2,98
|
7,28
|
7,64
|
N/A
|
0,07
|
|
SB
|
0,15
|
1,50
|
9,83
|
10,07
|
N/A
|
0,05
|
Fuente: elaboración propia
La precisión se evaluó mediante el análisis estadístico de la desviación estándar y el coeficiente de variación. Así, se evidenció que las medidas realizadas en los MCR presentaron valores inferiores a 0,15 en ambos laboratorios, lo que indicó una baja dispersión en los valores de pH, y por ende una buena precisión en los resultados obtenidos por el equipo (García, 2011). Los coeficientes de variación (% CV) también confirmaron el buen funcionamiento del equipo, ya que todos los porcentajes fueron inferiores al 10%, un valor considerado aceptable según (Gordón & Camargo, 2015).
Cabe destacar que tanto para el MCRa como para la solución SA (ambas de naturaleza ácida), los coeficientes de variación fueron más altos en ambos laboratorios en comparación con las demás sustancias. Estos valores evidenciaron la influencia de ciertos factores en las mediciones, en este caso principalmente el error ácido (Gómez et al., 2002). Este efecto se produce cuando los sensores de pH se saturan en soluciones muy ácidas, ya que los sitios de la superficie de vidrio se llenan de iones H+, reduciendo así la capacidad de medir el potencial eléctrico con precisión (Skoog, Holler & Nieman, 2009).
Sumado a lo anterior, se evidenció que los valores de desviación estándar y % CV para las tres soluciones de uso cotidiano fueron más altos en el Laboratorio 1 que en el laboratorio 2. Una razón de esta diferencia tiene que ver con el error de temperatura, puesto que, las soluciones medidas en el laboratorio 1 presentaron temperaturas superiores a los 25° C, a diferencia de las medidas realizadas en el laboratorio 2, con temperaturas inferiores. Si bien el equipo potenciométrico fue programado para realizar la compensación automática de temperatura, la respuesta del sensor pudo haber sido influenciada por la disociación de ácidos y bases o por la autodisociación del agua, un proceso en el cual dos moléculas de agua reaccionan entre sí para formar iones hidronio (H₃O+) e hidroxilo (OH-). Este equilibrio, sensible a los cambios de temperatura, puede alterar levemente la concentración de iones presentes en solución y, por ende, afectar las lecturas de pH (Douglas et al., 2015).
Según la revisión de literatura, para realizar la compensación de temperatura en este tipo de dispositivos analógicos, lo más recomendable es emplear sensores sumergibles como el DS18B20, según autores como Islam et al. (2022), Haziq et al. (2022), Salih et al. (2019), Soong et al. (2018), Lal et al. (2022), porque mejoran la precisión y exactitud de la medida, a diferencia de otros sistemas que han empleado sensores de temperatura ambiental como el DHT21 y LM35 (Collado et al., 2021; Sowmya et al., 2019).
Además, la robustez del equipo se evaluó mediante la prueba del Intervalo de Confianza (IC) al 99%. Los resultados indicaron que las mediciones son robustas, ya que los intervalos están próximos al valor de referencia de ambos MCR. Los valores obtenidos en el laboratorio 1 y en el laboratorio 2 mostraron pocas variaciones, sin influir significativamente en los resultados finales.
Para evaluar la exactitud del equipo se determinó el error relativo de los dos MCR, determinando un 97,24% para el MCRa y un 98,88% para el MCRn en el laboratorio 1 y 97,99% para el MCRa y 99,14% para el MCRn del laboratorio 2. Estos valores superaron los reportados en investigaciones similares, que han sido de 95,50%, 96,95% o menores al 90% (Megantoro et al., 2022; Promput et al., 2023).
En cuanto a la incertidumbre estándar de la media (UEM) para las soluciones de referencia en cada laboratorio, se observó que los valores de incertidumbre se mantuvieron alrededor de 0,03, a excepción de la incertidumbre del MCRa en el laboratorio 2, que fue de 0,05. A pesar de este leve incremento, las mediciones fueron consistentes y confiables.
En relación con los resultados de la UEM en soluciones de uso cotidiano, se observó que sus valores fueron superiores a los obtenidos en las mediciones de pH realizadas con los dos MCR. No obstante, la incertidumbre fue baja en todos los casos. La solución SA presentó menor incertidumbre en el laboratorio 1; la solución SN mostró valores idénticos en ambos laboratorios; y la solución SB evidenció mayor incertidumbre en el laboratorio 1.
Finalmente, cabe señalar que el equipo se calibró utilizando MCR del INM de Colombia, lo cual asegura que las mediciones de pH son trazables metrológicamente a las unidades del Sistema Internacional de Unidades, ya que dichas sustancias están vinculadas a materiales de referencia primarios del National Institute of Standards & Technology (NIST).
Componente pedagógico
Pretest
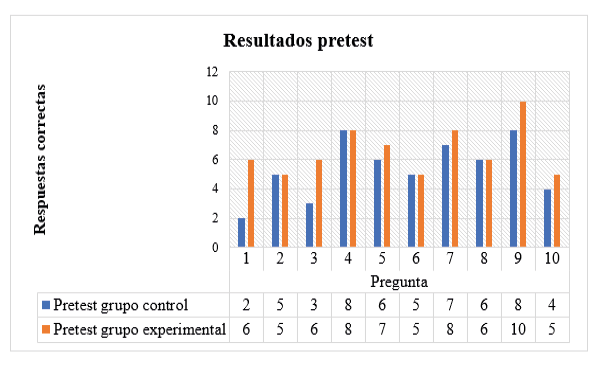
La siguiente figura presenta los resultados del pretest para los grupos control y experimental.
Figura 3. Resultados pretest
Fuente: Elaboración propia.
Teniendo en cuenta la frecuencia de respuestas correctas evidenciadas en la anterior figura, en cuanto a la pregunta 1, se pudo concluir que en el pretest los estudiantes presentaron debilidades en la conceptualización del pH; tan solo 8 de los 29 estudiantes participantes definieron correctamente el pH como -+. En cuanto a la pregunta 2, relacionada con el método de funcionamiento de una celda Harned para medir pH, 10 de los participantes señalaron la respuesta correcta, es decir, el método potenciométrico; por su parte, para la pregunta 3 se observó que tres de los estudiantes del grupo de control y 6 del grupo experimental relacionaron la pendiente de calibración de un electrodo de pH en soluciones buffer de pH con la pendiente teórica de la ecuación de Nernst. Para la pregunta 4, 8 estudiantes del grupo de control y 8 del grupo experimental conceptualizaron correctamente el significado de la trazabilidad metrológica del pH.
Para la pregunta 5, 13 de los participantes indicaron correctamente la pendiente de calibración de una sonda de pH, teniendo soluciones de referencia de 4,01 y 7,00. En el caso de la pregunta 6, se logró identificar que 5 de los participantes del grupo de control y 5 del experimental relacionan el valor de pH como variable dependiente de la temperatura.
Por otro lado, en la pregunta 7 se evaluó el conocimiento sobre la comprensión del funcionamiento de los equipos potenciométricos; en este sentido, 15 estudiantes de la totalidad respondieron correctamente. En el caso de la pregunta 8, se identificó que 12 de los estudiantes asociaron correctamente la unidad de mol con la constante de Avogadro y para la pregunta 9, 18 de los estudiantes participantes indicaron que el tipo de incertidumbre evaluada a partir de las mediciones directas es la de tipo A; por último, en la pregunta 10, se evidenció que tan solo 9 de los estudiantes diferenciaron la exactitud y la precisión en medidas de pH.
A partir de los resultados del pretest fue posible inferir que, aunque los participantes contaron con conocimientos previos asociados al concepto de pH, metrología y potenciometría, es importante generar estrategias didácticas para alcanzar una comprensión efectiva del concepto de pH, conocer las técnicas e instrumentos de medida del pH, y de manera predominante, la jerarquía metrológica reconocida para asociar el pH con el SI.
Posterior a la aplicación del pretest, para el grupo de control se realizaron sesiones teóricas donde magistralmente se abordaron temáticas asociadas a: concepto e historia de la definición del pH, trazabilidad metrológica del pH, funcionamiento y calibración de los sensores de pH, entre otros.
Para el caso del grupo experimental, además de realizar una sesión teórica sobre los temas abordados también con el grupo de control, se realizó un taller práctico, donde los estudiantes tuvieron la posibilidad de construir de manera grupal el hardware de un equipo potenciométrico y tomaron medidas con el equipo potenciométrico central de esta investigación. Las actividades prácticas con los estudiantes del grupo experimental, facilitaron la motivación por aprender conceptos asociados a otras ciencias como la ingeniería, la tecnología o la programación, ya que estas no han sido abordadas durante su formación académica. En la figura 4 se evidencia el trabajo práctico abordado con los estudiantes del grupo experimental.
Figura 4. Actividades con grupo experimental



Fuente: Elaboración propia.
Postest
En cuanto a los resultados de las respuestas correctas para el postest del grupo de control y el experimental, fue posible evidenciar una frecuencia más alta para el grupo experimental, lo cual permite concluir que la intervención a los estudiantes de este grupo mejoró su aprendizaje por temas relacionados al concepto de pH, trazabilidad metrológica del pH, potenciometría y relación del SI con el pH, principalmente.
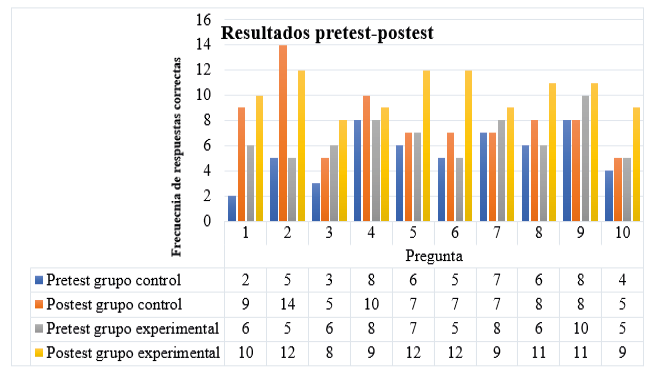
A continuación, en la figura 5 se muestra la frecuencia de respuestas correctas en el pretest y el postest para los grupos control y experimental; en esta se observa un incremento significativo en los resultados del grupo experimental después de la intervención.
Figura 5. Comparación respuestas correctas pretest y postest
Fuente: Elaboración propia.
Chi2Cy y Prueba Exacta de Fisher (PEF) del componente pedagógico
Los resultados de las pruebas Chi² con corrección de Yates y la Prueba Exacta de Fisher fueron interpretados según el valor p. Si p > 0,05, no se consideran diferencias significativas; en cambio, si p < 0,05, se interpreta que existen diferencias significativas a nivel estadístico. A continuación, la tabla 5 presenta los valores de p obtenidos en ambas pruebas, de acuerdo con los resultados del pretest y postest.
Tabla 5. Resultados prueba Chi2cy y PEF del componente pedagógico.
|
Pregunta
|
Prueba
|
Valor p
|
|
1
|
PEF
|
0,261
|
|
2
|
PEF
|
0,564
|
|
3
|
PEF
|
0,584
|
|
4
|
Chi2cy
|
0,854
|
|
5
|
Chi2cy
|
1,000
|
|
6
|
PEF
|
0,860
|
|
7
|
Chi2cy
|
0,843
|
|
8
|
Chi2cy
|
0,952
|
|
9
|
Chi2cy
|
0,851
|
|
10
|
PEF
|
0,804
|
Fuente: elaboración propia
De acuerdo a la tabla anterior, se puede evidenciar que el p valor para las preguntas 1, 2, 3 y 10 se realizó a través de la PEF. La prueba PEF se aplicó en estos casos, teniendo en cuenta que al realizar la prueba Chi2cy, al menos uno de los valores esperados de las respuestas correctas para el pretest y postest de los dos grupos fue menor a 5. Por su parte, las preguntas 4, 5, 7, 8 y 9 sí fueron analizadas según el modelo estadístico de Chi2cy.
En cuanto a los valores de p en la prueba Chi2cy, se evidencia que estos van de 0,843 a 1,000, lo cual es bastante alto y evidencian que no hubo prácticamente ninguna diferencia entre los grupos y los resultados obtenidos tanto en el pretest, como en el postest. Por otro lado, los valores de p en la PEF oscilaron entre 0,84 y 1,00, lo cual también sugiere que no hubo diferencias significativas en los resultados de los grupos.
Conclusiones
El equipo potenciométrico de código abierto desarrollado en esta investigación demostró ser versátil y confiable, permitiendo medir el pH en diversas soluciones con precisión. Su diseño portátil, la transmisión de datos vía Bluetooth o USB y la incorporación del sensor DS18B20 para compensación de temperatura contribuyeron a la flexibilidad y reducción de errores. Tras su calibración con Materiales de Referencia Certificada (MCR) del INM de Colombia, los resultados obtenidos fueron consistentes con los valores esperados, confirmando su eficacia para aplicaciones de medición potenciométrica.
El análisis estadístico mostró alta precisión, con bajas desviaciones estándar y un porcentaje de variación menor al 5%. La exactitud del equipo en soluciones de referencia fue sobresaliente, alcanzando un 99,84% en MCRa y 98,95% en MCRn, superando estudios previos y demostrando su confiabilidad en distintos entornos. Además, la baja incertidumbre estándar de la media (0,03 y 0,05) refuerza la estabilidad de las mediciones, lo que hace que el equipo sea adecuado para un uso experimental riguroso sin comprometer la calidad de los resultados.
En cuanto al componente pedagógico, según los resultados del pretest para el grupo de control y experimental, los participantes de la investigación, contaron con algunos conocimientos previos relacionados con pH, metrología, SI y potenciometría. Sumado a ello, a partir de la intervención pedagógica teórica-práctica con el grupo experimental, que incluyó la construcción de equipos potenciométricos con Arduino, se evidenció un incremento en las respuestas correctas para los resultados del postest, esto en comparación con el grupo de control; sin embargo, según las modelos Chi2cy y PEF, no se mostraron diferencias significativas, estadísticamente hablando.
Teniendo en cuenta lo anterior, se puede concluir que los instrumentos cuantitativos, como las pruebas estadísticas Chi2cy y PEF, ofrecen datos valiosos, pero no capturan completamente la complejidad de los fenómenos humanos, ya que se enfocan en variables medibles y descuidan aspectos subjetivos como emociones y motivaciones. Para obtener una comprensión más profunda, se recomienda complementar estos métodos con enfoques cualitativos, como entrevistas o grupos focales, que permitan explorar la experiencia subjetiva y las dinámicas sociales, brindando una visión más integral del fenómeno investigado.
Declaraciones finales
Contribución de los autores. Diana Yicela Pineda Caro: Adquisición de los recursos, Investigación, escritura, revisión y edición. Óscar Julio Medina Vargas: investigación, supervisión, redacción y revisión. Manuel Andrés Vélez Guerrero: investigación, supervisión y software.
Conflictos de interés. Los autores declaran que no tiene conflictos de interés.
Financiación. Este estudio fue financiado por el proyecto SGI 2892 “Cultura Metrológica: una Estrategia para el Desarrollo del Pensamiento Científico” de la Universidad Pedagógica y Tecnológica de Colombia.
Implicaciones éticas. Los autores declaran que este artículo no tiene implicaciones éticas.
Datos abiertos. Los autores declaran que no hay datos abiertos disponibles en el momento para el artículo.
Referencias
Álzate, E., Montes, J., & Escobar, R. (2012). Acondicionamiento del sensor de pH y temperatura para realizar titulaciones potenciométricas. Scientia et Technica, 2(51), 188–196.
Antończyk, A., Kiełbowicz, Z., Niżański, W., & Ochota, M. (2023). Comparison of 2 anesthetic protocols and surgical timing during cesarean section on neonatal vitality and umbilical cord blood parameters. BMC Veterinary Research, 19(1), 48. https://doi.org/10.1186/s12917-023-03607-2
Aoi, W., & Marunaka, Y. (2014). Importance of pH Homeostasis in Metabolic Health and Diseases: Crucial Role of Membrane Proton Transport. BioMed Research International, 2014, 1–8. https://doi.org/10.1155/2014/598986
Bartoš, D., Rewers, M., Wang, L., & Sørensen, T. (2022). Incorporating fluorescent nanomaterials in organically modified sol–gel materials – creating single composite optical pH sensors. Sensors & Diagnostics, 1(1), 185–192. https://doi.org/10.1039/D1SD00002K
Buck, R., Rondinini, S., Covington, A., Baucke, F., Brett, C., Camoes, M., Milton, M., Mussini, T., Naumann, R., Pratt, K., Spitzer, P., & Wilson, G. (2002). Measurement of pH. Definition, standards, and procedures (IUPAC Recommendations 2002). Pure and Applied Chemistry, 74(11), 2169–2200. https://doi.org/10.1351/pac200274112169
Collado, E., Valdés, E., García, A., & Sáez, Y. (2021). Design and implementation of a low-cost IoT-based agroclimatic monitoring system for greenhouses. AIMS Electronics and Electrical Engineering, 5(4), 251–283. https://doi.org/10.3934/electreng.2021014
Cristancho, R., & Castillo, A. (2020). Automation of Secondary pH-Measurement System at National Metrology Institute of Colombia. 2020 International Conference on Electrical, Communication, and Computer Engineering (ICECCE), June, 1–4. https://doi.org/10.1109/ICECCE49384.2020.9179242
Dey, K., & Sheth, M. (2023). Development of Galactooligosaccharide (GOS) added gummies: sensory, characterization and shelf quality. Food Production, Processing and Nutrition, 5(1), 8. https://doi.org/10.1186/s43014-022-00117-w
Douglas, A., Skoog, F., & Holler, J. (2015). Principios de análisis instrumental. Mc Graw Hill.
García, C. (2011). Estadística Descriptiva y Probabilidades para Ingenieros. Empresa Editorial Macro.
Gill, T., & Zheng, X. (2020). Comparing Methods for Quantifying Electrochemically Accumulated H2O2. Chemistry of Materials, 32(15), 6285–6294. https://doi.org/10.1021/acs.chemmater.0c02010
Gómez, S., Soria, E., & Vivó, M. (2002). Análisis electroquímico. Revista de Diagnóstico Biológico, 51(1), 18–27.
Gordón, R., & Camargo, I. (2015). Selección de estadísticos para la estimación de la precisión experimental en ensayos de maíz. Agronomía Mesoamericana, 26(1), 55. https://doi.org/10.15517/am.v26i1.16920
Grupo Hanna Instruments. (2020). ¿Está cometiendo errores en la medición de pH? https://www.hannacolombia.com/blog/post/88/esta-cometiendo-errores-en-la-medicion-ph#
Haziq, M., Pang, W. L., Chan, K. Y., Lee, I. E., Chung, G. C., & Wong, S. K. (2022). High-efficiency Low-cost Smart IoT Agriculture Irrigation, Soil’s Fertility and Moisture Controlling System. Universal Journal of Agricultural Research, 10(6), 785–793. https://doi.org/10.13189/ujar.2022.100616
Hindayani, A., Hamim, N., Elishian, C., Aristiawan, Y., Mulyana, M. R., Handayani, E. M., Pratiwi, E., & Ginanjar, G. (2021). Establishment of Traceability Chain For pH Measurement in Indonesia. IOP Conference Series: Materials Science and Engineering, 1011(1), 012059. https://doi.org/10.1088/1757-899X/1011/1/012059
Islam, M., Kashem, M., & Uddin, J. (2022). An internet of things framework for real-time aquatic environment monitoring using an Arduino and sensors. International Journal of Electrical and Computer Engineering (IJECE), 12(1), 826. https://doi.org/10.11591/ijece.v12i1.pp826-833
Julian, J., Wahyuni, F., & Ulhaq, F. D. (2023). Reliability Analysis of pH Measurement on TLC4502 with E201C Electrodes based on ATmega328P Microcontroller: Approach to Analysis of Variation with ANOVA. ELKHA, 15(1), 32. https://doi.org/10.26418/elkha.v15i1.62982
Khan, M., Mukherjee, K., Shoukat, R., & Dong, H. (2017). A review on pH sensitive materials for sensors and detection methods. Microsystem Technologies, 23(10), 4391–4404. https://doi.org/10.1007/s00542-017-3495-5
Kicińska, A., Pomykała, R., & Izquierdo, M. (2022). Changes in soil pH and mobility of heavy metals in contaminated soils. European Journal of Soil Science, 73(1). https://doi.org/10.1111/ejss.13203
Lal, P., Prakash, A., Chand, A., Prasad, K., Mehta, U., Assaf, M., Mani, F., & Mamun, K. (2022). IoT integrated fuzzy classification analysis for detecting adulterants in cow milk. Sensing and Bio-Sensing Research, 36, 100486. https://doi.org/10.1016/j.sbsr.2022.100486
Li, H., Long, J., Jing, H., & Xiao, J. (2023). Steering from electrochemical denitrification to ammonia synthesis. Nature Communications, 14(1), 112. https://doi.org/10.1038/s41467-023-35785-w
Lunelli, B., & Scagnolari, F. (2009). pH Basics. Science and Education, 86(2), 1–5.
Mccarty, C., & Maynard, J. (2006). pH Paradoxes : Demonstrating that it is not true that pH ≡ -log [ H+]. Journal of Chemical Education, 83(5), 752–757.
Megantoro, P., Prastio, R., Kusuma, H., Abror, A., Vigneshwaran, P., Priambodo, D., & Alif, D. (2022). Instrumentation system for data acquisition and monitoring of hydroponic farming using ESP32 via Google Firebase. Indonesian Journal of Electrical Engineering and Computer Science, 27(1), 52. https://doi.org/10.11591/ijeecs.v27.i1.pp52-61
Pineda, D. Y., Medina, Ó. J., & Falla, G. (2020). Enseñanza del concepto de pH desde la perspectiva del pensamiento científico: una revisión sistemática exploratoria. Pensamiento y Acción, 30, 37–51. https://doi.org/10.19053/01201190.n30.2021.12129
Promput, S., Maithomklang, S., & Panya-isara, C. (2023). Design and Analysis Performance of IoT-Based Water Quality Monitoring System using LoRa Technology. TEM Journal, 29–35. https://doi.org/10.18421/TEM121-04
Ricoy, C. (2006). Contribución sobre los paradigmas de investigación. Educação Revista do Centro de Educação. 31(1), 11–22. https://www.redalyc.org/pdf/1171/117117257002.pdf
Salih, N., Hasan, I., & Abdulkhaleq, N. (2019). Design and implementation of a smart monitoring system for water quality of fish farms. Indonesian Journal of Electrical Engineering and Computer Science, 14(1), 44. https://doi.org/10.11591/ijeecs.v14.i1.pp44-50
Samešová, D., Poništ, J., Hybská, H., Pochyba, A., Schwarz, M., & Salva, J. (2023). Determination of aerobic and anaerobic biological degradability of waste tyres. Environmental Sciences Europe, 35(1), 19. https://doi.org/10.1186/s12302-023-00723-6
Sánchez, F. (2019). Fundamentos epistémicos de la investigación cualitativa y cuantitativa : consensos y disensos. Revista Digital de Investigación, 13(1), 102–122. https://doi.org/https://doi.org/10.19083/ridu.2019.644
Santos, W., & Cavalheiro, É. (2015). Assembling and Using an LED-Based Detector To Monitor Absorbance Changes during Acid-Base Titrations. Journal of Chemical Education, 92(10), 1709–1715. https://doi.org/10.1021/ed500931p
Simha, P., Vasiljev, A., Randall, D. G., & Vinnerås, B. (2023). Factors influencing the recovery of organic nitrogen from fresh human urine dosed with organic/inorganic acids and concentrated by evaporation in ambient conditions. Science of the Total Environment, 879, 163053. https://doi.org/10.1016/j.scitotenv.2023.163053
Skoog, D., Holler, F. J., & Nieman, T. (2009). Principios de Análisis Instrumental. Cengage Learning.
Soong, R., Agmata, K., Doyle, T., Jenne, A., Adamo, T., & Simpson, A. (2018). Combining the maker movement with accessibility needs in an undergraduate laboratory: A cost-effective text-to-speech multipurpose, Universal Chemistry Sensor Hub (MUCSH) for students with disabilities. Journal of Chemical Education, 95(12), 2268–2272. https://doi.org/10.1021/acs.jchemed.8b00638
Sowmya, D., Praveen, R., & Govardhan, K. (2019). Smart Water Dripping System for Agriculture/ Farming. International Journal of Recent Technology and Engineering, 8(2S10), 876–881. https://doi.org/10.35940/ijrte.B1161.0982S1019
Zambrano, N., Camelo, E., Méndez, A., & Valderrama, Y. (2019). Diseño e implementación de un instrumento electrónico de medida de PH para terreno agrícola. Investigacion e Innovación En Ingenierias, 7(1), 110–132. https://doi.org/10.17081/invinno.7.1.3042
Zhang, W., Yang, S., Li, Q., Fan, D., & Li, Y. (2023). Broadening the pH range of molecular oxygen activation for zero-valent aluminum by ball-milling surface modification. Applied Surface Science, 622, 156881. https://doi.org/10.1016/j.apsusc.2023.156881
.png)